I/ TESTS D’IDENTIFICATION DES ANIONS ET DES CATIONS :
I-1/ COULEURS DE QUELQUES IONS EN SOLUTION AQUEUSE :

I-2/ COULEUR DE QUELQUES IONS AU TEST A LA FLAMME :
Le test consiste à introduire un échantillon de l’ion à l’aide d’un fil de platine dans une flamme, non lumineuse et à haute température (bec de bunsen), puis à observer la couleur qu’on obtient.
I-2-1/ TEST A LA FLAMME DE L’ION CUIVRE II (Cu2+) :
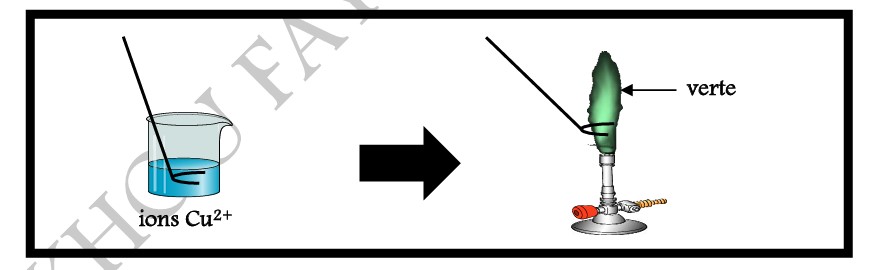
I-2-2/ TEST A LA FLAMME DE L’ION CALCIUM II (Ca2+) :
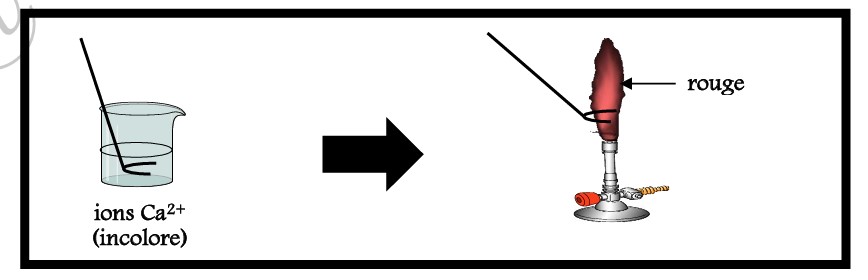
I-2-3/ TEST A LA FLAMME DE L’ION BARYUM (Ba2+) :
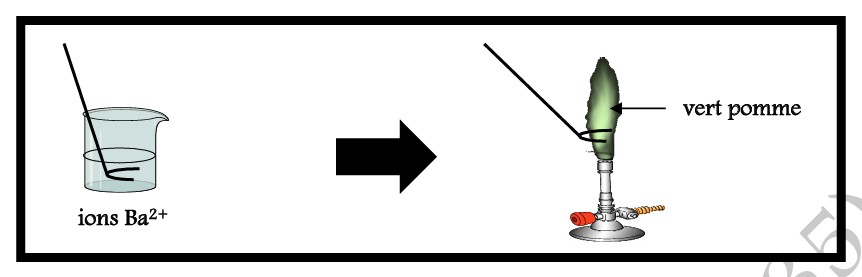
I-2-4/ TEST A LA FLAMME DE L’ION SODIUM (Na+) :

I-2-5/ TEST A LA FLAMME DE L’ION ZINC (Zn2+) :

I-2-5/ TEST A LA FLAMME DE L’ION PLOMB (Pb2+) :
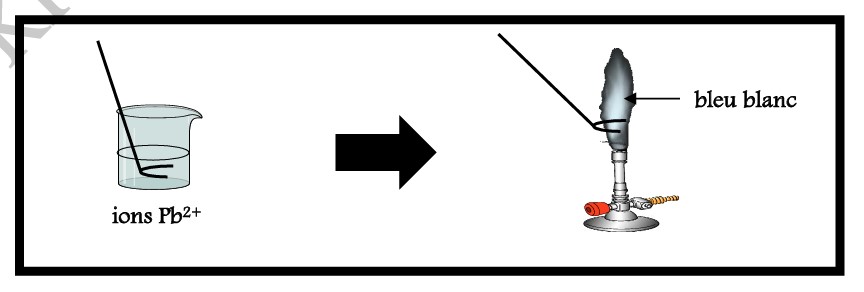
I-2-6/ TEST A LA FLAMME DE L’ION POTASSIUM (K+) :

I-3/ REACTIONS DE PRECIPITATION :
I-3-1/ DEFINITION D’UN PRECIPITE :
Un précipité est un solide insoluble résultant de la réaction chimique entre un anion et un cation. La couleur du précipité dépend des ions qui réagissent.
I-3-2/ EXEMPLES DE REACTIONS DE PRECIPITATION :
Le test consiste à verser quelques gouttes d’une solution renfermant d’ions précipitateurs (qui jouent le rôle de réactif) dans un tube à essai contenant l’ion à identifier (ions précipités), puis à observer la couleur du précipité qu’on obtient.
La formation du précipité résulte de l’incompatibilité en solution entre l’ion à identifier et l’ion qui joue le rôle de réactif.
I-3-2-1/ REACTIONS DE PRECIPITATION ENTRE L’ION Cu2+ ET L’ION HO- :

I-3-2-2/ REACTIONS DE PRECIPITATION ENTRE L’ION Fe2+ ET L’ION HO- :

I-3-2-3/ REACTIONS DE PRECIPITATION ENTRE L’ION Fe3+ ET L’ION HO- :

I-3-2-4/ REACTIONS DE PRECIPITATION ENTRE L’ION Zn2+ ET L’ION HO- :

I-3-2-5/ REACTIONS DE PRECIPITATION ENTRE L’ION Al 3+ ET L’ION HO- :

I-3-2-6/ REACTIONS DE PRECIPITATION ENTRE L’ION Cl – ET L’ION Ag+ :

I-4/ REDISSOLUTION DE CERTAINS PRECIPITES :
L’identification de certains ions nécessite pour la plupart des tests complémentaires appelés tests de confirmation.
I-4-1/ TEST COMPLEMENTAIRE DES IONS Zn2+ :
Le précipité d’hydroxyde de zinc se redissout dans un excès de soude ou d’ammoniac.
Ce qui se traduit par les équations bilan suivantes :

I-4-2/ TEST COMPLEMENTAIRE DES IONS Al 3+ :
Le précipité d’hydroxyde d’aluminium se redissout dans un excès de soude mais pas dans l’ammoniac.
Ce qui se traduit par l’équation bilan suivante :
![]()
AlO2- est appelé ion aluminate
II/ ORGANIGRAMME DE RECHERCHE DES IONS :

You must be logged in to take the quiz.

