I/ CONSTITUANT DE LA MATIERE :
I-1/ ELEMENT CHIMIQUE :
I-1-1/ MISE EN EVIDENCE DE L’ELEMENT CARBONE :
I-1-1-1/ PYROLYSE DU SUCRE :
Chauffons quelques morceaux de sucre dans un tube à essai.

Nous observons:
► La formation d’un résidu noir au fond du tube: le sucre renferme l’élément chimique, le carbone.
► La formation de gouttelettes d’eau sur les parois du tube.
I-1-1-2/ LA COMBUSTION DE BUTANE :
La combustion d’un corps consiste à bruler ce corps dans du dioxygène de l’air.
Brûlons du gaz butane dans le dioxygène de l’air.
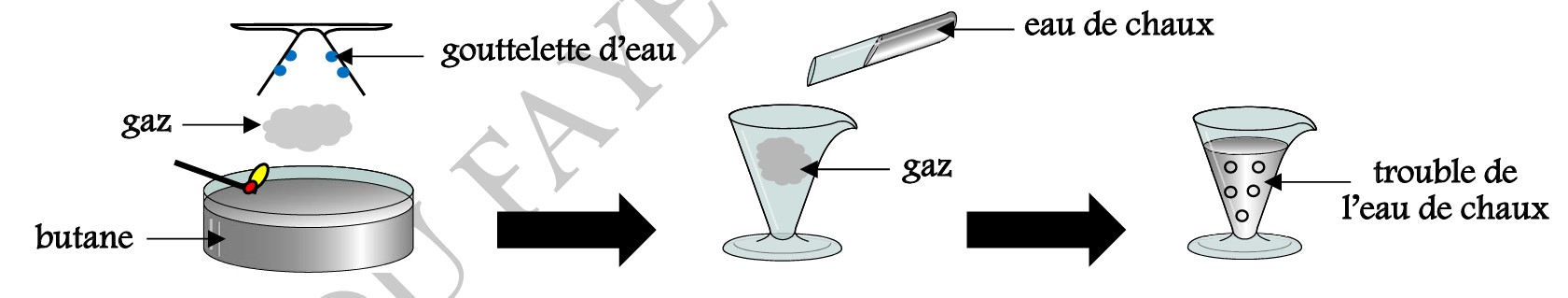
Nous observons:
► La formation d’un gaz qui trouble l’eau de chaux. Ce gaz est le dioxyde de carbone mettant en évidence
l’élément chimique le carbone dans le butane.
► La formation de gouttelettes d’eau sur les parois du tube.
I-1-2/ MISE EN EVIDENCE DE L’ELEMENT HYDROGENE :
Dans les deux expériences précédentes, on note la formation de gouttelette d’eau: ce qui montre que le sucre
comme le butane renferme l’élément chimique, l’hydrogène.
I-1-3/ NOTION D’ELEMENT CHIMIQUE :
Un élément chimique est un constituant commun à un ensemble de cors purs.
I-1-4/ SYMBOLE D’UN ELEMENT CHIMIQUE :
Dans la nature il existe une centaine d’éléments chimiques distincts. Les chimistes conviennent de
représenter chaque élément par un symbole.
► En générale le symbole de l’élément chimique est la première lettre en majuscule du nom de l’élément.
Exemples:
Hydrogène (H) ; Bore (B) ; Carbone (C) ; oxygène (O) ; Fluor (F) ; Soufre (S)…
► Si d’autres éléments commencent par la même lettre, alors on ajoute une deuxième lettre en minuscule à la lettre majuscule.
Exemples:
Hélium (He) ; Béryllium (Be) ; Calcium (Ca) ; Chlore (Cl) ; Fer (Fe) ; Aluminium (Al)…
► Certains éléments ont conservé le symbole de leur ancien nom latin.
Exemples:
Azote (N) ; Sodium (Na) ; Potassium (K) ; Mercure (Hg) ; Or (Au)…
I-2/ ATOMES :
I-2-1/ HISTORIQUE :
Le mot atome vient du mot grec «atomos» qui veut dire insécable c’est-à-dire indivisible. De nombreuses
expériences ont montrées qu’il était possible de scinder l’atome en d’autres particules plus fines.
► C’est ainsi qu’en 1881 JJ Thomson découvre l’un des composants de l’atome ; il s’agit de particules
élémentaires négatives appelées en 1891 électrons.
► En 1932 Chadwick a découvert le neutron.
► En 1904, Thomson partant de l’idée que l’atome est électriquement neutre pense qu’il doit contenir des charges positives qui compensent les charges négatives des électrons.
► En 1912 Rutherford bombarde différents échantillons de matières (Cuivre, Or, Argent) avec des
particules et il déduit de son expérience que la charge positive doit occuper un tout petit volume qu’il appelle noyau.
► Au cours de la même année, Heisenberg a fait l’hypothèse que les noyaux atomiques sont formés de
protons et de neutrons.
I-2-2/ MODELE ATOMIQUE :
L’atome est assimilé à une sphère formée d’une partie centrale appelée noyau chargé positivement et une
partie périphérique appelée nuage ou cortège électronique chargé négativement.

II/ STRUCTURE DE L’ATOME :
II-1/ CONSTITUANTS DE L’ATOME :
L’atome est constitué de trois particules élémentaires: les protons, les neutrons et les électrons.
II-1-1/ LE NOYAU ATOMIQUE :
Le noyau de l’atome est constitué de deux types de particules élémentaires: les protons et les neutrons dont l’ensemble est appelé nucléons.
Chaque noyau est caractérisé par:
► Le nombre de proton noté (Z), ce nombre est aussi appelé nombre de charge ou numéro atomique.

► Le nombre de neutron noté (N)
![]()
N.B:
► Le nombre de nucléon ou nombre de masse noté (A) est :
► La charge du noyau est:
► La masse du noyau est:
Si mρ = mn alors ;
II-1-2/ LE NUAGE ELECTRONIQUE :
Le nuage électronique d’un atome est constitué de particules élémentaires appelé électron.
REMARQUE :
Dans un atome le nombre d’électrons du nuage électronique est toujours égale au nombre de protons (Z) du noyau.
II-2/ NUCLEIDE :
On désigne par nucléide l’ensemble des noyaux d’un même élément chimique ayant la même valeur de Z
et la même valeur de A. Il est représenté par:
X : représente le symbole de l’élément
A : représente le nombre de nucléon
Z : représente le nombre de proton
![]()
II-3/ NUCLEIDES ISOTOPES:
Des nucléides sont dits isotopes lorsqu’ils ont les mêmes nombres de protons mais des nombres de nucléons différents.

II-4/ POURCENTAGE OU ABONDANCE ISOTOPIQUE:
Exemples de l’élément carbone:

II-5/ STRUCTURE LACUNAIRE DE L’ATOME:

REMARQUE:
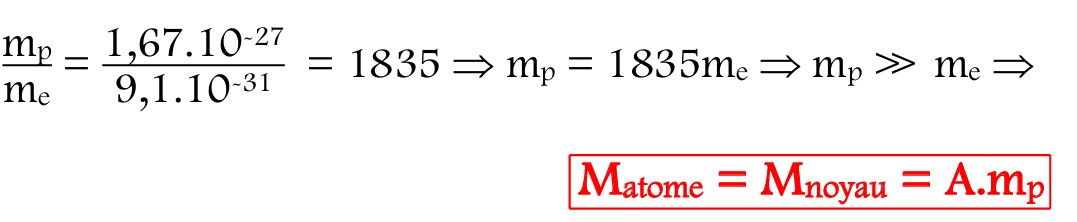
La masse d’un atome est sensiblement égale à celle de son noyau alors que le rayon du noyau est 105 fois plus petit que celui du l’atome. Il se passe comme si la masse est concentrée dans un petit volume et le reste est occupé par le vide : on dit que l’atome présente une structure lacunaire.
II-6/ CHARGE D’UN ATOME :
L’atome est électriquement neutre.
II-7/ STRUCTURE OU CONFIGURATION ELECTRONIQUE DE L’ATOME :
Les électrons du cortège électronique d’un atome se répartissent sur des couches électroniques ou niveau d’énergie. Chaque couche est caractérisée par une lettre. Les trois premières couches sont représentées
successivement par les lettres K, L, M correspondants respectivement aux nombres entiers 1, 2, 3 appelés
nombres quantiques.
II-7-1/ REGLES DE REMPLISSAGE :
La répartition des électrons obéit à certaines règles:
Première règle :
Un niveau de rang n contient au maximum 2n² électrons
► La couche K (première couche n = 1) peut contenir un maximum de 2 électrons.
► La couche L (deuxième couche n = 2) peut contenir un maximum de 8 électrons.
► La couche M (troisième couche n = 3) peut contenir un maximum de 18 électrons.
N.B: lorsqu’une couche est pleine, on dit qu’elle est saturée.
Deuxième règle :
Le remplissage des couches électroniques s’effectue en commençant par la couche K. Lorsqu’elle est saturée on remplit la couche L et ainsi de suite.
II-7-2/ CONFIGURATION (STRUCTURE) ELECTRONIQUE (S.E) ET FORMULE ELECTRONIQUE (F.E) :
Etablir la configuration électronique (ou structure électronique) d’un atome revient à préciser la répartition des électrons de cet atome dans les différents couches électroniques. Pour cela on représente les couches par des cases et les électrons par des points.
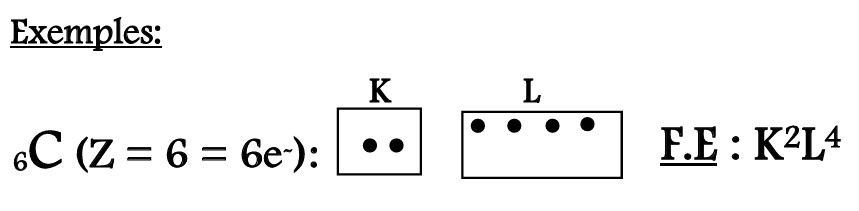
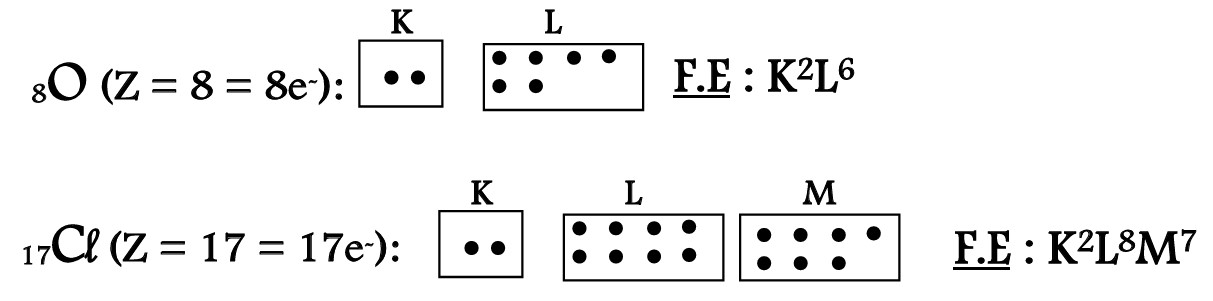
II-7-3/ STRUCTURE OU SCHEMA DE LEWIS D’UN ATOME :
Etablir le schéma de Lewis d’un atome consiste à répartir les électrons de la dernière couche autour du symbole de l’élément.
Les électrons célibataires sont représentés par des points et les électrons appariés par des tirets.
Exemples:

II-7-4/ VALENCE D’UN ATOME :
C’est le nombre d’électrons célibataire dans la structure de Lewis de l’atome.
Exemples:
Valence du carbone est égale à 4. Valence de l’oxygène est égale à 2. Valence du chlore est égale à 1.
III/ CLASSIFICATION PERIODIQUE :
III-1/ PRINCIPE :
On connait aujourd’hui avec certitude 112 éléments. Les 112 éléments chimiques sont rangés en lignes par
numéros atomiques (Z) croissant. La classification comporte 7 lignes, également appelées périodes et 18
colonnes (numérotés de 1 à 18) également appelées groupes.
III-2/ TABLEAU SIMPLIFIE :
Le tableau simplifié comporte 8 colonnes ou groupes et 7 lignes aussi appelées périodes.
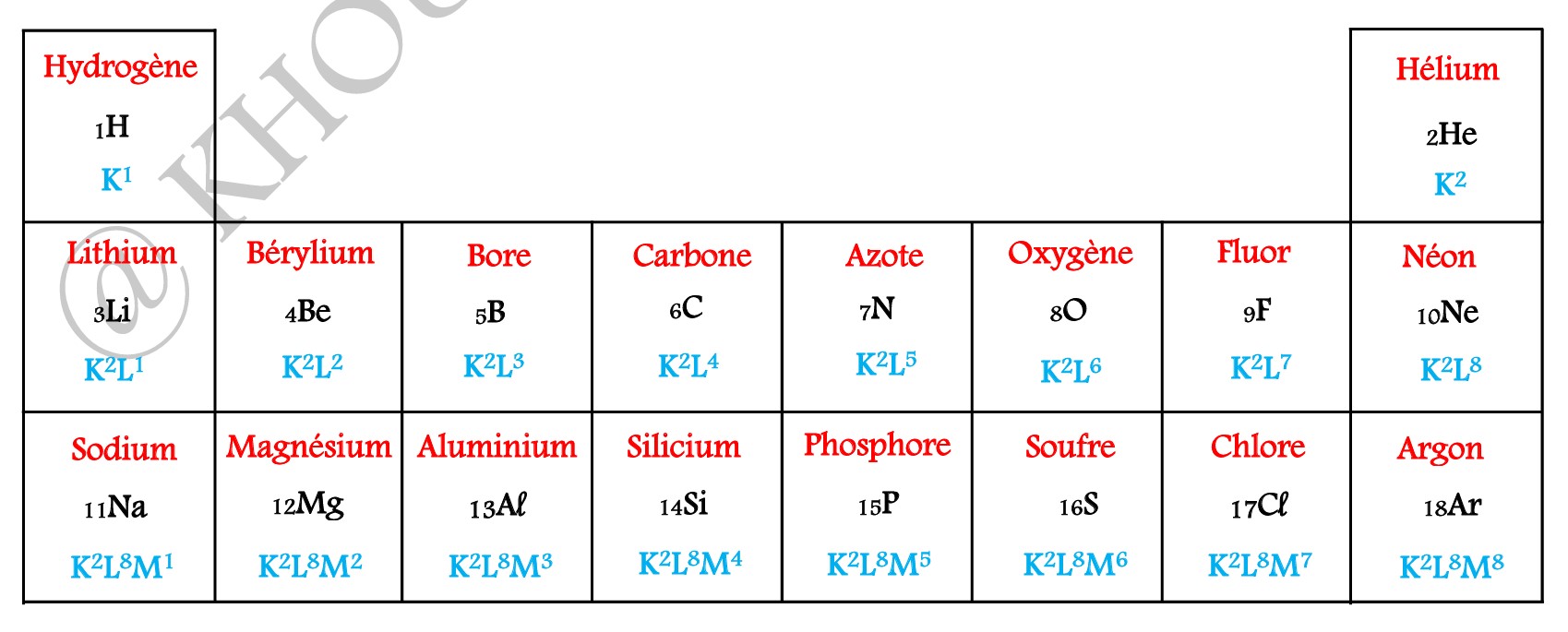
III-3/ COLONNE ET PERIODE :
III-3-1/ COLONNE OU GROUPE :
Le numéro de la colonne de l’atome correspond au nombre d’électrons dans sa couche externe.
III-3-2/ PERIODE OU LIGNE :
Le numéro de la période de l’atome correspond au nombre de couches électroniques occupées.
III-4/ FAMILLES D’ELEMENTS CHIMIQUES :
Les éléments chimiques ayant des propriétés chimiques semblables sont regroupés dans une même colonne formant ainsi une famille d’éléments chimiques. Parmi les familles d’éléments chimiques, on distingue:
► La famille des métaux alcalins: ce sont les éléments de la première colonne sauf l’hydrogène.
► La famille des alcalinoterreux: ce sont les éléments de la deuxième colonne.
► La famille des halogènes: ce sont les éléments de la septième colonne.
► La famille des gaz rares: ce sont les éléments de la huitième colonne.
IV/ STABILITE DES ATOMES : REGLE DU « DUET » ET DE L’OCTET :
IV-1/ REGLE DU « DUET » :
Au cours de leurs transformations chimiques, les atomes de numéros atomiques inférieurs à 6 (Z < 6) évoluent de manière à acquérir un « duet » d’électrons. Ils acquièrent ainsi la structure de l’hélium.
IV-2/ REGLE DE L’OCTET :
Au cours de leurs transformations chimiques, les atomes de numéros atomiques supérieurs à 6 (Z > 6) évoluent de manière à acquérir un octet d’électrons sur leur couche externe. Ils acquièrent ainsi la structure du gaz rare la plus proche.
N.B: La règle de l’octet permet de prévoir la charge d’un ion monoatomique.
V/ ION MONOATOMIQUE :
V-1/ DEFINITION :
On appelle ion monoatomique un atome chargé positivement ou négativement.
Contrairement aux atomes le nombre d’électrons d’un ion monoatomique est différent du numéro atomique (Z) de l’atome correspondant.
On distingue deux types d’ions monoatomiques.
V-2/ IONS POSITIFS OU CATIONS :
On appelle ions positif ou cations un atome chargé positivement c’est-à-dire un atome qui perd des électrons.
Les éléments des colonnes (I ; II et III) peuvent perdre respectivement (un électron; deux électrons et trois électrons) et prennent la forme des gaz rares les plus proches.
Exemples :

![]()
N.B:
Nombre d’électrons d’un cation = numéro atomique (Z) de l’atome correspondant – nombre d’électrons perdus
Exemples :
Nombre d’électrons (11Na+) = 11 – 1 = 10 électrons
Nombre d’électrons (4Be²+) = 4 – 2 = 2 électrons
Nombre d’électrons (13Al 3+) = 13 – 3 = 10 électrons
V-3/ IONS NEGATIFS OU ANIONS :
On appelle ions négatif ou anions un atome chargé négativement c’est-à-dire un atome qui gagne des électrons.
Les éléments des colonnes (VII ; VI et V) peuvent gagner respectivement (un électron ; deux électrons et trois électrons) et prennent la forme des gaz rares les plus proches.
Exemples :
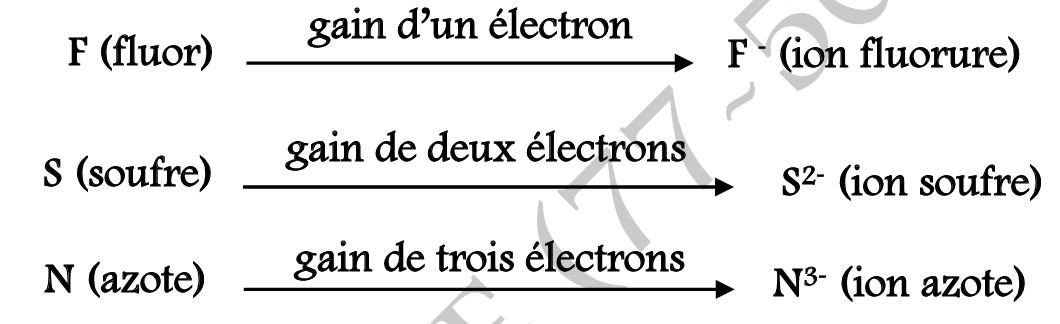
N.B:
Nombre d’électrons d’un anion = numéro atomique (Z) de l’atome correspondant + nombre d’électrons gagnés.
Exemples:
Nombre d’électrons (9F -) = 9 + 1 = 10 électrons
Nombre d’électrons (16S²-) = 16 + 2 = 18 électrons
Nombre d’électrons (7N3-) = 7 + 3 = 10 électrons
You must be logged in to take the quiz.




