I/ LIAISON COVALENTE :
I-1/ DEFINITION :
Une liaison covalente résulte de la mise en commun d’électrons célibataires provenant de deux atomes.
On distingue trois types de liaisons covalentes:
► Liaison covalente simple : c’est une mise en commun de deux électrons célibataires entre deux atomes.
Exemple :
![]() ► Liaison covalente double : c’est une mise en commun de quatre électrons célibataires entre deux atomes.
► Liaison covalente double : c’est une mise en commun de quatre électrons célibataires entre deux atomes.
Exemple :
![]()
► Liaison covalente triple : c’est une mise en commun de six électrons célibataires entre deux atomes.
Exemple :
![]()
REMARQUE :
Un atome peut établir autant de liaisons covalentes qu’il possède d’électrons célibataires dans son schéma
de Lewis.
Exemples :

I-2/ MOLECULE :
I-2-1 DEFINITION :
On appelle molécule tout édifice chimique, électriquement neutre ; formé d’atomes liés entre eux par des
liaisons covalentes.
N.B: dans une molécule tous les atomes doivent avoir un octet d’électrons (huit électrons) autour d’eux sauf l’hydrogène qui doit en avoir autour de lui un duet d’électrons (deux électrons)
I-2.2/ FORMULE BRUTE :
La formule brute d’une molécule est constituée des symboles des différents éléments affectés en indice de coefficient indiquant leur nombre dans la molécule.
Exemples :
molécule d’eau (H2O) ; molécule d’ammoniac (NH3) ; molécule d’éthanol (C2H6O) ; molécule de méthane (CH4)…
I-2-3/ ATOMICITE D’UNE MOLECULE :
L’atomicité d’une molécule représente le nombre d’atome qu’elle renferme.
Exemple :
![]()
I-2-4/ REPRESENTATION DE LEWIS D’UNE MOLECULE :
La représentation de Lewis d’une molécule est une représentation des atomes et de tous les doublets d’électrons périphériques liants et non liants (libres) de cette molécule.
I-2-5/ LA FORMULE DEVELOPPEE ET LA SEMI DEVELOPPEE D’UNE MOLECULE :
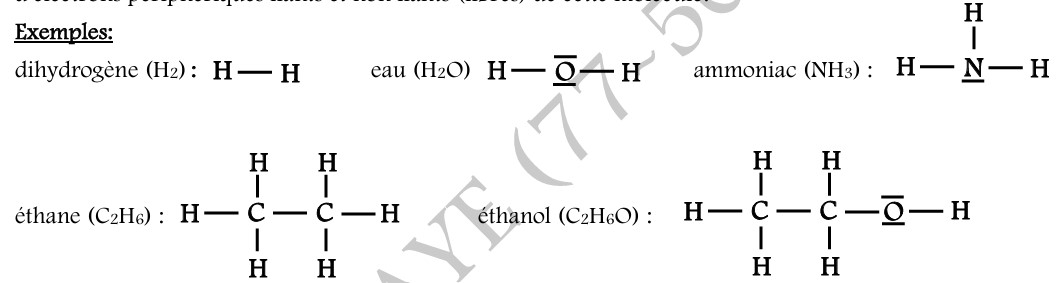
I-2-5-1/ LA FORMULE DEVELOPPEE :
La formule développée d’une molécule est une représentation de Lewis de la molécule où les doublets non
liants ne sont pas représentés.
I-2-5-2/ LA FORMULE SEMI DEVELOPPEE :
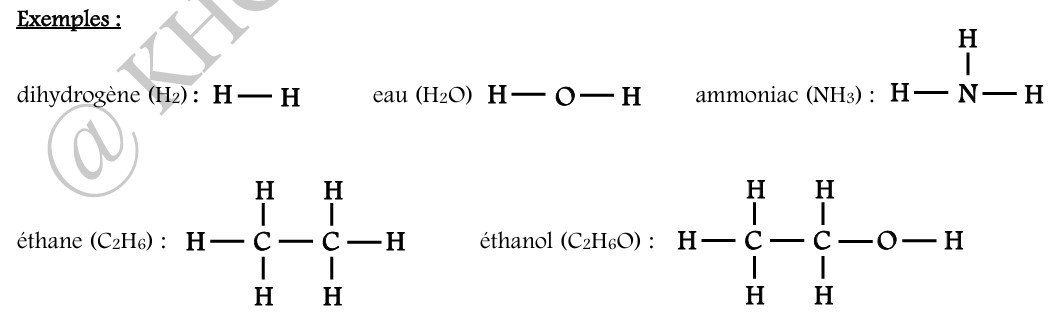
La formule semi développée est une écriture simplifiée de la formule développée dans laquelle les liaisons
de types X — H (O — H ; N — H ; C — H …) ne sont pas représentées.
Exemples:
![]()
I-3/ L’ELECTRONEGATIVITE, ELECTROPOSITIVITE :
I-3-1/ L’ELECTRONEGATIVITE :
L’électronégativité est la tendance d’un atome à capter des électrons.
I-3-2/ L’ELECTROPOSITIVITE :
L’électropositivité est la tendance d’un atome à céder des électrons.
I-4/ LIAISON COVALENTE POLARISEE ET LIAISON COVALENTE NON POLARISEE :
I-4-1/ LIAISON COVALENTE POLARISEE :
Lorsqu’une liaison covalente s’établit entre 2 atomes d’électronégativité différente, le doublet électronique liant se déplace du côté de l’atome le plus électronégativité (la paire d’électron est en moyenne plus proche de l’atome le plus électronégatif): la liaison formée est dite polarisée.
Exemples:

I-4-2/ LIAISON COVALENTE NON POLARISEE :
Lorsqu’une liaison covalente s’établit entre 2 atomes de même électronégativité : la liaison formée est dite non polarisée.
Exemples:
![]()
I-5/ LIAISON DATIVE :
Une liaison dative est une description de liaison covalente entre deux atomes pour lesquels les deux électrons partagés dans la liaison proviennent du même atome.

II/ LIAISON IONIQUE :
II-1/ DEFINITION :
Une liaison ionique est un transfert d’un électron célibataire d’un atome électropositif vers un atome électronégatif.
II-2/ EXEMPLES QUELQUES IONS :
II-2-1/ IONS MONOATOMIQUES :

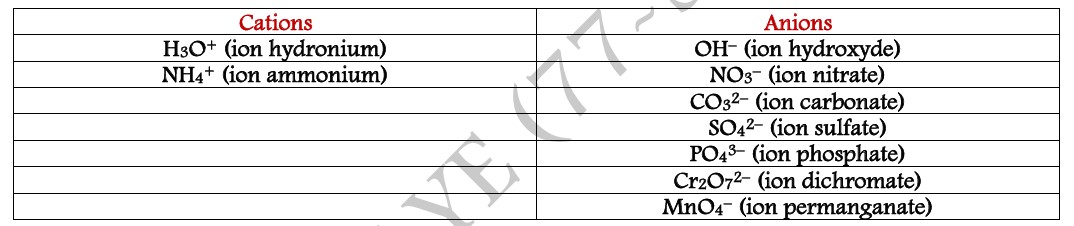
II-2-2/ IONS POLYATOMIQUES :
Un ion polyatomique est un ion formé à partir de plusieurs atomes.
II-3/ NOM D’UN COMPOSE IONIQUE:
Un composé ionique est formé d’un cation et d’un anion.
Pour donner le nom d’un composé ionique, on procède ainsi:
![]()
Exemples:

II-4/ FORMULE IONIQUE ET FORMULE STATISTIQUE D’UN COMPOSE IONIQUE :
Soit un composé ionique formé des ions Xp+ et Yq – où p et q sont des entiers compris entre 1 et 3.

Exemples:
► Chlorure de calcium: ![]()


III/ STRUCTURE DE LA MATIERE :
III-1/ ETAT DESORDONNE :
On note les états désordonnés dans les molécules liquides et gazeuses car: les molécules liquides s’empilent
de façon désordonnés et glissent les unes sur les autres et les molécules gazeuses sont animés de mouvements
désordonnés dans toutes les directions.
III-2/ ETAT ORDONNE: LA STRUCTURE CRISTALLINE :
A l’état ordonné il n’existe que des molécules solides.
You must be logged in to take the quiz.

