I/ LA MOLE :
I-1/ NOTION DE MOLE :
Déterminons le nombre d’atomes de fer contenu dans une masse m = 3,48 g de fer.
► On cherche d’abord la masse d’un atome de fer:![]()
► Calculons le nombre d’atomes de fer dans les 3,48 g :
![]()
On constante que la masse m = 3,48 g de fer contient d’énormes quantités d’atomes de fer, d’où la nécessité d’introduire une nouvelle échelle plus commode.
Ainsi, pour passer de l’échelle atomique à l’échelle macroscopique, les chimistes sont convenus de les compter par «paquets» contenant chacun le même nombre d’entités chimiques élémentaires (atomes ; molécules ; ions ; électrons…): un tel «paquet» s’appelle une mole.
I-2/ DEFINITION:
La mole, unité de la quantité de matière est la quantité de matière contenant autant d’entités élémentaires dans un «paquet».
La quantité de matière ou nombre de mole est noté par n et s’exprime en mol.
I-3/ NOMBRE OU CONSTANTE D’AVOGADRO :
On appelle nombre ou constante d’Avogadro le nombre d’entités chimiques élémentaire contenus dans une mole. Il est noté N ou NA.
![]()
Exemples :
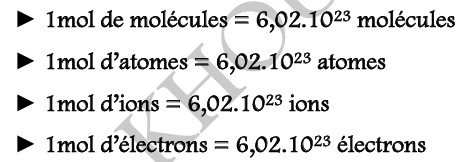
REMARQUE :
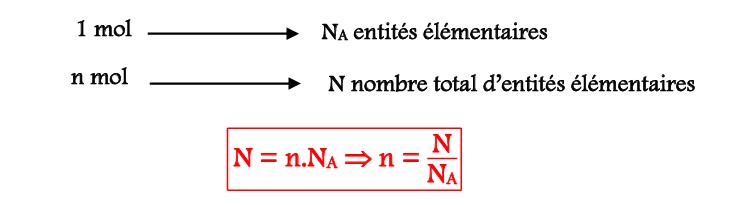
La constante d’Avogadro (NA) permet de déterminer la quantité de matière (n) en mol correspondante à un nombre donné d’entités chimiques élémentaires (N).
II/ GRANDEURS MOLAIRES :
II-1/ MASSE MOLAIRE :
II-1-1/ DEFINITION GENERALE :
La masse molaire d’une espèce est la masse d’une mole d’entités de cette espèce. Elle est notée M et s’exprime en gramme par mole![]()
II-1-2/ MASSE MOLAIRE ATOMIQUE :
La masse molaire atomique est la masse d’une mole d’atome.
Exemples:
![]()
REMARQUE :
La masse molaire d’un ion monoatomique est égale à la masse molaire de l’atome correspondant.
Exemple:
![]()
II-1-3/ MASSE MOLAIRE MOLECULAIRE :
La masse molaire moléculaire est la masse d’une mole de molécule de cette espèce. Elle est égale à la somme des masses molaires atomiques des atomes présents dans la molécule.
Exemple:
![]()
II-1-4/ MASSE MOLAIRE MOYENNE :
Les corps naturels sont en général pour un élément donné, constitués de mélanges d’isotopes. Seul l’or (Au) et le phosphore (P) sont formés à partir d’atomes absolument identiques.
Le pourcentage d’un isotope dans l’échantillon est appelé abondance relative ou isotopique.
Ainsi pour déterminer la masse molaire moyenne notée M d’un élément X constitué d’isotopes X1, X2, …,Xn ayant respectivement les pourcentages isotopiques %(X1), %(X2) , …, %(Xn), on applique l’expression suivante: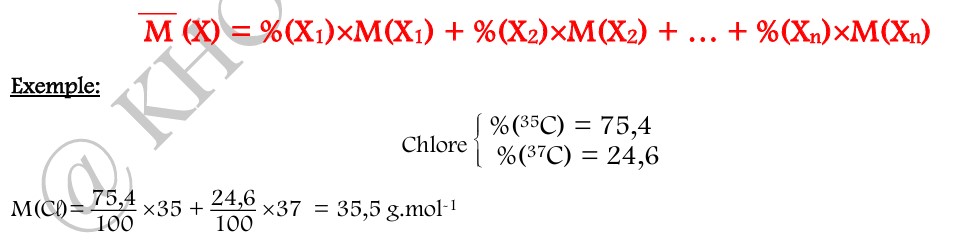
II-2/ MASSE MOLAIRE ET QUANTITE DE MATIERE :
La quantité de matière (n) d’un corps pur de masse molaire (M) possède une masse (m) définie par: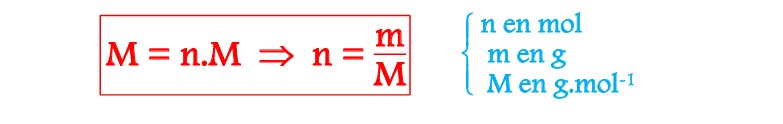
II-3/ COMPOSITION OU POURCENTAGE CENTESIMALE:
II-3-1/ COMPOSITION CENTESIMALE MASSIQUE:
Le pourcentage en masse d’un élément dans un composé est la masse de cet élément contenu dans 100 g de ce composé.
Exemple:
Pour le composé: CxHyOz ![]()
Dans le cas où le nombre de mole du composé est égale à 1 mole alors la masse du
composé est égale à sa masse molaire.
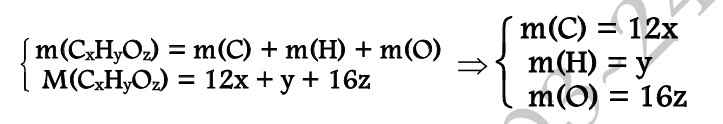 Ainsi on peut réécrire
Ainsi on peut réécrire

REMARQUE:
La relation qui lie les nombres d’atomes (x, y, z) et les compositions centésimales massiques des différents éléments est appelée relation de proportionnalité. Elle est définie par:
![]()
II-3-2/ COMPOSITION CENTESIMALE MOLAIRE OU POURCENTAGE ATOMIQUE :
Le pourcentage centésimal molaire d’un élément dans un composé est le nombre d’atomes de cet élément contenu dans 100 atomes de ce composé.
Exemple: CxHyOz
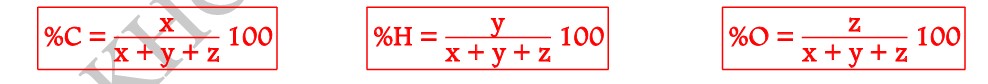
III/ VOLUME MOLAIRE :
III-1/ EQUATION D’ETAT DES GAZ PARFAITS :
Un gaz parfait est un gaz qui obéit à l’équation d’état des gaz parfaits:

REMARQUE :

AUTRES UNITES DE LA PRESSION :
1 bar = 105 Pa
1 atm = 1,013 bar = 1,013 105 Pa = 76 cm de mercure = 760 mm de mercure
III-2/ VOLUME MOLAIRE D’UN GAZ :
Le volume molaire d’un corps pur gazeux est le volume d’une mole de ce corps. Il dépend de la température et de la pression. Il est noté Vm et s’exprime en m3.mol-1 dans le système international.
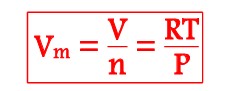
REMARQUE :
Dans les conditions normales de température et de pression (C.N.T.P) c’est-à-dire pression P = 1atm et température T = 0°C = 273 K alors:
![]()
III-3/ GAZ ET QUANTITE DE MATIERE :
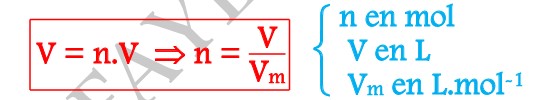
La quantité de matière (n) d’un corps pur gazeux de volume molaire (Vm) occupe un volume (V) défini
par:
III-4/ LOI D’AVOGADRO-AMPERE :
Des volumes égaux de gaz pris dans les mêmes conditions de températures et de pression renferment le même nombre de moles.
IV/ DENSITE D’UN GAZ :
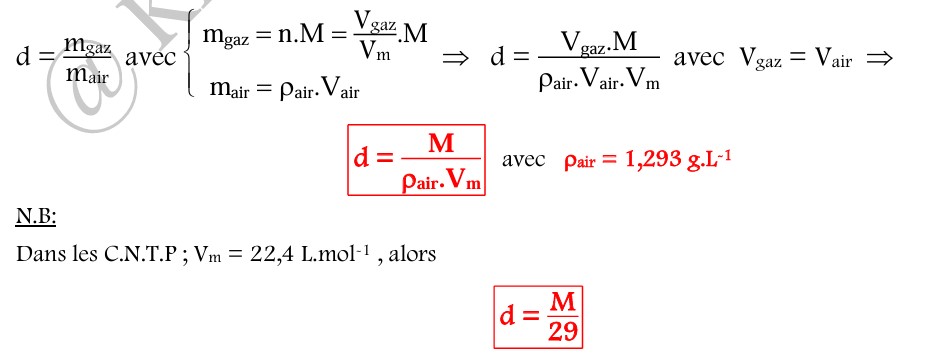
La densité d’un gaz par rapport à l’air est le rapport de sa masse sur la masse d’un égal volume d’air.
You must be logged in to take the quiz.

