I/ REACTIONS CHIMIQUES :
I-1/ EXEMPLES DE REACTIONS CHIMIQUES :
I-1-1/ COMBUSTION DU CARBONE DANS LE DIOXYGENE :
Plaçons un morceau de charbon de bois incandescent dans une enceinte contenant du dioxygène et de l’eau de chaux.
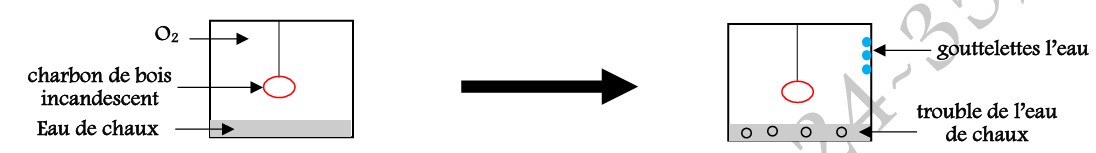 Observations :
Observations :
La combustion du charbon de bois donne de l’eau (H2O) et un gaz qui trouble l’eau de chaux, le dioxyde de carbone (CO2).
I-1-2/ REACTION ENTRE LE FER ET LE SOUFRE :
Plaçons un mélange de fer et de soufre sur une brique puis chauffons ce mélange.
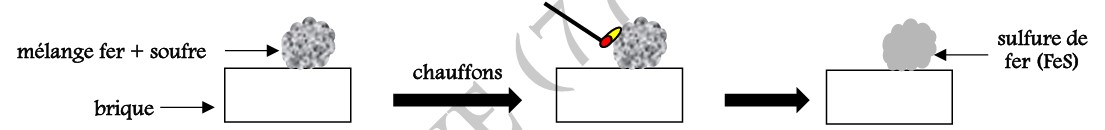
Observations :
En mélangeant du fer et du soufre puis en chauffant ce mélange, on obtient un solide gris: c’est le sulfure de fer (FeS).
I-2/ DEFINITION :
Une réaction chimique est une transformation chimique au cours de laquelle un ou des corps pur(s) appelé(s) réactif(s) se transforme (ent) en un ou des corps pur(s) appelé(s) produit(s).
Ι-3/ CARACTERISTIQUES D’UNE REACTION CHIMIQUE :
I-3-1/ ASPECT ENERGETIQUE :
Les réactions chimiques peuvent se produire:
► Avec un dégagement de chaleur: elles sont dites exothermiques.
Exemple : combustion du charbon de bois.
► Avec absorption de chaleur: elles sont dites endothermiques.
Exemple : dissolution du chlorure d’ammonium dans l’eau.
►sans absorption ni dégagement de chaleur: elles sont dites athermiques.
Exemple : dissolution du chlorure de sodium
I-3-2/ ASPECT CINETIQUE :
Il existe des réactions chimiques rapides (exemples: réactions de précipitation, action de l’acide chlorhydrique sur le zinc…) et des réactions chimiques lentes (exemples: transformation du fer en rouille, saponification (fabrication du savon)…)
I-4/ LOI DE CONSERVATION :
I-4-1/ LOI DE CONSERVATION DE LA MASSE OU LOI DE LAVOISIER :
Au cours d’une réaction chimique la somme des masses des réactifs transformés est égale à la somme des masses des produits formés.
I-4-2 LOI DE CONSERVATION DES ATOMES :
Au cours d’une réaction chimique les éléments chimiques présents au niveau des réactifs sont les mêmes éléments chimiques que l’on retrouve au niveau des produits après transformation.
II/ EQUATION-BILAN D’UNE REACTION CHIMIQUE :
II-1/ ECRITURE DE L’EQUATION-BILAN D’UNE REACTION CHIMIQUE:
Une réaction chimique est représentée par une équation-bilan. Les espèces chimiques y sont représentées par leurs formules brutes.
► Les espèces chimiques qui entrent en réaction appelées réactifs sont écrites dans le membre de gauche de l’équation.
► Les espèces chimiques qui sont formées par la réaction appelées produits sont écrites dans le membre de droite.
► Enter les réactifs et les produits, on place une flèche qui indique le sens de l’évolution de la réaction.
Réactif (s) → Produit (s)
II-2/ EQUILIBRAGE D’UNE EQUATION-BILAN D’UNE REACTION CHIMIQUE :
Pour équilibrer une équation-bilan, on multiplie les formule brutes par des coefficients appelés coefficients stœchiométriques afin d’assurer la conservation des atomes, de la masse et des charges.
II-3/ DOUBLE SIGNIFICATION DE L’EQUATION-BILAN D’UNE REACTION CHIMIQUE :
Prenons l’exemple de la synthèse de l’eau:
![]()
Signification microscopique: Deux molécules de dihydrogène réagissent avec une molécule de dioxygène pour donner deux molécules d’eau.
Signification macroscopique: Deux moles de molécules de dihydrogène réagissent avec une mole de molécule de dioxygène pour donner deux moles de molécule d’eau.
II-4/ RELATION DE PROPORTIONNALITE ENTRE LES NOMBRES DE MOLES MIS EN JEU DANS UNE REACTION CHIMIQUE:
Soit la réaction chimique d’équation bilan suivante:
![]()
Lors d’une réaction chimique, on a toujours la relation de proportionnalité (appelé aussi bilan molaire):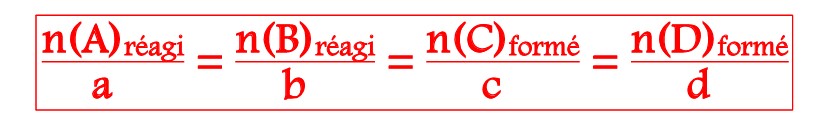
III/ RENDEMENT D’UN PRODUIT D’UNE REACTION CHIMIQUE :
Le rendement d’un produit d’une réaction chimique est le rapport entre la masse expérimentale de ce produit sur la masse théorique de ce produit.

►La masse expérimentale est la masse synthétisée: elle est déterminée par pesée du produit formé.
►La masse théorique est la masse calculée à partir de la masse des réactifs.
You must be logged in to take the quiz.

