I/ PHENOMENE DE DISSOLUTION :
I-1/ MISE EN EVIDENCE :

I-1-1/ OBSERVATION :
Après avoir mélangé et bien agité, le sucre n’est plus visible dans l’eau: il se forme ainsi un mélange homogène:
I-1-2/ CONCLUSION :
On dit que le sucre s’est dissout dans l’eau: c’est le phénomène de dissolution. Le mélange homogène ainsi obtenu est appelé solution.
N.B:
► Dans une solution, le corps qui dissout est appelé solvant et le (s) corps qui est (sont) dissout (s) est (sont) appelé (s) soluté (s).
► Le soluté peut être solide, liquide ou gazeux.
I-2/ DEFINITION :
On appelle solution un mélange homogène constitué d’un solvant et d’un (ou plusieurs) soluté.
REMARQUE :
Lorsque le solvant est l’eau, la solution obtenue est dite solution aqueuse.
I-3/ SOLUTIONS AQUEUSES IONIQUES ET SOLUTIONS AQUEUSES NON IONIQUES :
I-3-1/ SOLUTIONS AQUEUSES IONIQUES :
Une solution aqueuse est ionique lorsqu’elle conduit le courant électrique: une telle solution contient des ions (cations et anions). Le soluté est un composé ionique.
Exemple : mélange entre l’eau et le sel de cuisine (NaCl) ; mélange entre l’eau et la soude (NaOH) ….
I-3-1/ SOLUTIONS AQUEUSES NON IONIQUES:
Une solution aqueuse est non ionique lorsqu’elle ne conduit pas le courant électrique: une telle solution ne contient pas d’ions. Le soluté est un composé moléculaire.
Exemples: mélange entre l’eau et le sucre.
II/ ROLES DU SOLVANT ET EFFETS THERMIQUES:
II-1/ ROLES DU SOLVANT:
II-1-1/ ROLE DISSOCIANT :
Lorsqu’on dissout un composé ionique (NaCl) dans l’eau, l’eau détruit la liaison ionique entre les atomes de Na et Cl, on obtient ainsi une solution ionique contenant les ions Na+ et Cl-: l’eau est un solvant dissociant.
II-1-2/ ROLE IONISANT :
Lorsqu’on dissout un composé moléculaire (HCl) dans l’eau, l’eau détruit la liaison covalente entre les atomes de H et Cl, on obtient ainsi une solution ionique contenant les ions H+ et Cl-: l’eau est un solvant ionisant.
II-1-3/ ROLE DE SOLVATATION :
Lorsqu’en solution, chaque ion est entouré de molécules du solvant, celles-ci forment un bouclier et empêchent toute interaction entre les ions: on dit que le solvant a un rôle de solvatation.
REMARQUES :
► Dans le cas où le solvant est l’eau la solvatation porte le nom d’hydratation.
► Certains cristaux ioniques peuvent capter des molécules d’eau de l’atmosphère et s’hydrater. Leur formule brute fait apparaitre cette hydratation.
Exemple: sulfate de cuivre hydraté (CuSO4 ; 5H2O)
II-2/ EFFETS THERMIQUES DE LA DISSOLUTION :
► Une dissolution qui n’absorbe ni ne dégage de la chaleur est dite athermique (NaCl dans l’eau).
► Une dissolution qui absorbe de la chaleur est dite endothermique (NH4Cl dans l’eau).
► Une dissolution qui dégage de la chaleur est dite exothermique (NaOH dans l’eau).
III/ GRANDEURS CARACTERISTIQUES DES SOLUTIONS AQUEUSES :
III-1/ CONCENTRATION MASSIQUE D’UNE SOLUTION AQUEUSE (CM) :
C’est la masse m de soluté contenue dans un volume V de solution.

III-2/ CONCENTRATION MOLAIRE D’UNE SOLUTION AQUEUSE (C) :
C’est la quantité de matière n de soluté contenue dans un volume V de solution.
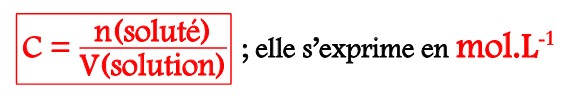
III-3/ RELATION ENTRE Cm ET C :
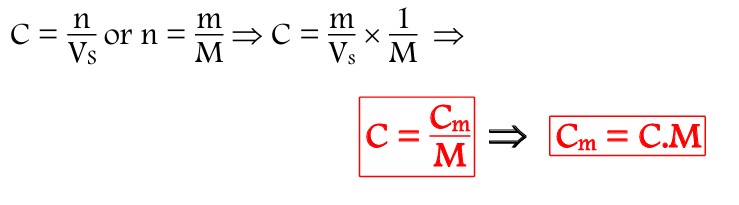
III-4/ SOLUBILITE D’UN SOLUTE DANS L’EAU :
C’est la quantité maximale de soluté que l’on peut dissoudre dans un volume d’eau. C’est une grandeur qui dépend de la température.
III-5/ SATURATION D’UNE SOLUTION :
Une solution est dite saturée lorsque le soluté ne peut plus se dissoudre dans le solvant (eau).
IV/ PREPARATION DE SOLUTIONS :
IV-1/ CAS OU LE SOLUTE EST UN SOLIDE :
Le principe consiste à dissoudre une masse m du soluté solide dans un volume V d’eau bien précis.
Exemple: préparation d’une solution de soude de concentration molaire volumique C = 10-2 mol.L-1 et de volume V = 500 mL.
IV-1-1/ DETERMINATION DE LA MASSE M A DISSOUDRE :
![]()
IV-1-2/ MODE OPERATOIRE :
A l’aide d’une balance, on pèse une masse m = 0,2 g de soude qu’on place ensuite dans une fiole jaugée de 500 mL. On ajoute ensuite un peu d’eau dans la fiole pour dissoudre le solide. Une fois la soude dissoute dans l’eau, on ajoute de l’eau jusqu’au trait de jauge.
IV-2/ CAS OU LE SOLUTE EST UN LIQUIDE (SOLUTION COMMERCIALE) :
Le principe consiste à diluer un volume V0 de la solution commerciale de concentration C0 par un volume V d’eau bien précis.
Expression de C0:

Exemple:
Préparation d’une solution d’acide chlorhydrique de concentration molaire volumique
C = 10-2 mol.L-1 et de volume V = 500 mL à partir d’une solution mère de concentration C0 = 1 mol.L-1.
IV-2-1/ DETERMINATION DU VOLUME V0 A DILUE :
Lors d’une dilution le nombre de mole ne varie pas.

IV-2-2/ MODE OPERATOIRE:
On prélève à l’aide d’une pipette jaugée de la solution mère un volume V0 = 5 mL qu’on place ensuite dans une fiole jaugée de 500 mL. On ajoute un peu d’eau dans la fiole pour ensuite agiter. Une fois le mélange homogène, on ajoute de l’eau jusqu’au trait de jauge.
You must be logged in to take the quiz.

