I/ SOLUTIONS ACIDES, BASIQUES ET NEUTRES :
I-1/ EXPERIENCE :
Considérons des tubes à essais contenant différentes solutions aqueuses. Dans chaque tube, introduisons quelques gouttes de Bleu de Bromothymol (B.B.T).

I-2/ OBSERVATIONS :
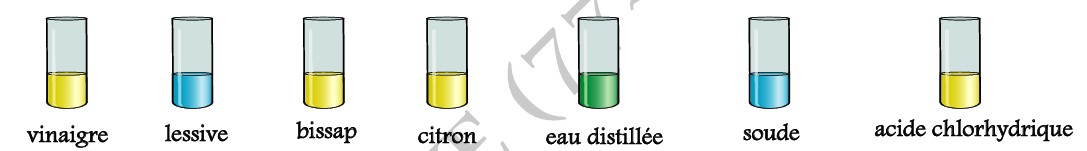
Le B.B.T prend alors les colorations suivantes:
I-3/ CONCLUSIONS :
On peut donc classer les solutions aqueuses en 3 catégories:
► Les solutions qui font virer le B.B.T au jaune sont qualifiées de solutions acides.
Exemples: vinaigre, bissap, citon, acide chlorhydrique…
► Les solutions qui font virer le B.B.T au bleu sont qualifiées de solutions basiques.
Exemples: soude, lessive…
► Les solutions qui font virer le B.B.T au vert sont qualifiées de solutions neutres.
Exemples: eau distillée…
II/ L’ACIDE CHLORHYDRIQUE :
II-1/ PREPARATION DE D’ACIDE CHLORHYDRIQUE :
II-1-1/ LE CHLORURE D’HYDROGENE :
II-1-1-1/ STRUCTURE :
Le chlorure d’hydrogène est un gaz moléculaire de formule HCl. La liaison covalente entre l’atome d’hydrogène et l’atome de chlore est polarisée (fragile) du fait de la différence d’électronégativité.
II-1-1-2/ PROPRIETES PHYSIQUES :
Dans les conditions ordinaires de température et de pression, le chlorure d’hydrogène est un gaz incolore d’odeur piquante, très irritant pour les voies respiratoires. Il est plus dense que l’air.
II-1-2/ PREPARATION DU CHLORURE D’HYDROGENE :
II-1-2-1/ EXPERIENCE:
Le principe consiste à ajouter une solution d’acide sulfurique (H2SO4) sur du chlorure de sodium (NaCl) en chauffant légèrement.

II-1-2-2/ OBSERVATION :
On constate un dégagement de gaz qu’on peut recueillir par déplacement d’air.
II-1-2-3/ INTERPRETATION :
Le gaz qui se dégage est du chlorure d’hydrogène, il provient de la réaction entre l’acide sulfurique et le chlorure de sodium.
L’équation bilan de la réaction s’écrit:
![]()
II-1-3/ DISSOLUTION DU GAZ CHLORHYDRIQUE: EXPERIENCE DU JET D’EAU :
Le principe consiste à remplir d’abord du chlorure d’hydrogène gazeux dans un ballon, ensuite on place quelques gouttes d’eau distillée dans l’un des orifices du bouchon traversé par un tuyau souple ; l’autre extrémité du tuyau est hermétiquement fermée par une pince. En fin on retourne le ballon au-dessus d’un cristallisoir contenant de l’eau distillée additionnée de bleu de bromothymol puis retire la pince:
immédiatement après on voit apparaitre un puissant jet d’eau dans le ballon.

II-2/ PROPRIETES DE LA SOLUTION D’ACIDE CHLORHYDRIQUE :
II-2-1/ CONDUCTIBILITE ELECTRIQUE :
II-2-1-1/ EXPERIENCE :
Réalisons le circuit ci-dessous. L’électrolyseur contient une solution d’acide chlorhydrique.

II-2-1-2/ OBSERVATION :
On constate que l’ampoule brille quand on forme l’interrupteur
II-2-1-3/ INTERPRETATION :
La solution d’acide chlorhydrique conduit le courant électrique donc elle contient des ions. Lors de la dissolution l’eau a totalement ionisé les molécules de chlorure d’hydrogène selon l’équation-bilan:
![]()
II-2-1-4/ CONCLUSION :
La solution d’acide chlorhydrique contient alors des ions hydroniums (H3O+) et des ions chlorures (Cl -).
N.B:
► Les ions hydroniums (H3O+) sont responsables du caractère acide d’une solution acide.
► La solution d’acide chlorhydrique sera notée: (H3O+ + Cl -)
II-2-2/ PROPRIETES DES IONS HYDRONIUMS (H3O+) :
II-2-2-1/ ACTION SUR LES METAUX :
Les ions hydroniums peuvent réagir avec certains métaux (zinc, aluminium, fer, plomb, nickel…) pour donner du dihydrogène (H2) de l’eau (H2O) et l’ion correspondant au métal.
Exemples:
► Réaction entre les ions hydroniums (H3O+) et le zinc métal (Zn) :
![]()
► Réaction entre les ions hydroniums (H3O+) et l’aluminium métal (Al) :
![]()
II-2-2-2/ ACTION SUR LES INDICATEURS COLORES :
Un indicateur coloré est une substance qui ajouté dans une solution (acide, basique ou neutre) vire pour donner des colorations différentes.
► Expérience :
Considérons trois tubes à essais contenant chacun une solution d’acide chlorhydrique. Puis ajoutons dans chaque tube un indicateur coloré (hélianthine tube 1 ; phénolphtaléine tube 2 et B.B.T tube 3).
 ► Observations :
► Observations :

On constate que la solution dans le tube (1) vire au rouge ; la solution dans le tube (2) reste incolore et la solution dans le tube (3) vire au jaune.
► Interprétation:
Les couleurs obtenus caractérisent la présence des ions hydroniums (H3O+) dans ces solutions.
II-2-2-3/ ACTION SUR LES BASES :
Les ions hydroniums (H3O+) réagissent également avec les bases.
Nous traiterons ces réactions dans le chapitre suivant.
II-2-3/ REACTION DE CARACTERISATION DE L’ION CHLORURE (Cl -):
L’action du nitrate d’argent (Ag+ ; NO3-) sur une solution d’acide chlorhydrique (H3O+ ; Cl -) donne un précipité blanc, le chlorure d’argent (AgCl) qui noircit à la lumière: la solution d’acide chlorhydrique contient des ions chlorures (Cl -).
L’équation bilan de la réaction est:

III/ ACIDES COURANTS ET PRODUITS NATURELS ACIDES :
III-1/ DEFINITION :
Un acide est une espèce chimique capable de libérer un ou plusieurs protons H+ en solution (chaque proton H+ est ionisé par une molécule d’eau (H2O) pour donner un ion hydronium H3O+).
On distingue les monoacides et les polyacides:
► Lorsqu’une mole d’acide peut libérer une mole d’ions H+ : l’acide est qualifié de monoacide.
Exemples :
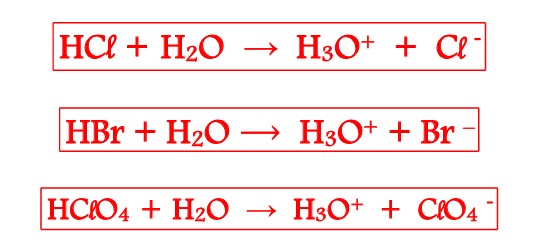 ► Lorsqu’une mole d’acide peut libérer deux moles d’ions H+: l’acide est qualifié de diacide.
► Lorsqu’une mole d’acide peut libérer deux moles d’ions H+: l’acide est qualifié de diacide.
Exemples :
![]()
III-2/ LES ACIDES COURANTS :
III-2-1/ EXPERIENCE :
Considérons trois tubes à essais contenant respectivement une solution d’acide nitrique, une solution d’acide sulfurique et une solution d’acide éthanoïque. Dans chaque tube, introduisons quelques gouttes de Bleu de Bromothymol (B.B.T).

III-2-2/ OBSERVATIONS :
On constante que toutes les solutions d’acide font virer le B.B.T au jaune.

III-2-3/ INTERPRETATION :
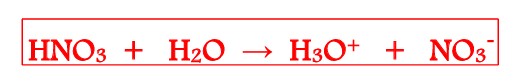
Les solutions d’acide nitrique, d’acide sulfurique et d’acide éthanoïque contiennent tous des ions hydroniums (H3O+): ce sont donc des acides.
Les équations bilan de ces acides dans l’eau sont:

III-3/ LES PRODUITS ACIDES NATURELS :
III-3-1/ EXPERIENCE :
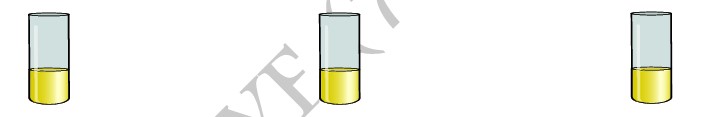
Considérons trois tubes à essais contenant respectivement du jus de bissap, du jus de tamarin et du jus de citron. Puis ajoutons dans chaque tube du B.B.T.

III-3-2/ OBSERVATIONS :
On constante que toutes ces solutions de jus font virer le B.B.T au jaune.
III-3-3/ INTERPRETATION :
Ces extraits naturels contiennent tous des ions hydroniums (H3O+): ce sont donc des acides.
You must be logged in to take the quiz.

