I/ SOLUTIONS BASIQUES :
I-1/ EXPERIENCE :
Considérons deux tubes à essais contenant respectivement des solutions aqueuses de lessive et de la soude.
Dans chaque tube, introduisons quelques gouttes de Bleu de Bromothymol (B.B.T).

I-2/ OBSERVATIONS :
Les solutions dans les deux tubes virent à la coloration bleue:

I-3/ CONCLUSIONS :
On peut donc dire que les solutions de lessive et de soude sont des solutions basiques.
II/ STRUCTURE ET PROPRIETES DU CRISTAL D’HYDROXYDE DE SODIUM (SOUDE) :
II-1/ STRUCTURE DU CRISTAL D’HYDROXYDE DE SODIUM :
Elle est constituée d’un empilement ordonné d’ions hydroxyde (OH-) et d’ions sodium (Na+).
II-2/ PROPRIETES DU CRISTAL D’HYDROXYDE DE SODIUM :
► L’hydroxyde de sodium est un solide blanc vendu sous forme de pastilles ou billes blanches.
Sa formule statistique est NaOH.
► Laisser à l’air libre, l’hydroxyde de sodium absorbe l’humidité de l’air: on dit qu’il est hygroscopique.
► L’hydroxyde de sodium peut se désagréger et devenir liquide en absorbant l’humidité de l’air: on parle de déliquescence de l’hydroxyde de sodium
III/ SOLUTION D’HYDROXYDE DE SODIUM :
III-1/ DISSOLUTION DE L’HYDROXYDE DE SODIUM :
III-1-1/ EXPERIENCE :
Ajoutons quelques grammes d’hydroxyde de sodium dans un tube à essai contenant de l’eau puis agitons le tube.
III-1-2/ OBSERVATIONS ET CONCLUSIONS:
On constate:
► Que les quelques grammes d’hydroxyde de sodium ont disparus: on dit que l’hydroxyde de sodium s’est dissout facilement dans l’eau.
► Une augmentation de la température au niveau du tube à essai lors de cette dissolution: on dit que la dissolution est exothermique.
III-2/ ELECTROLYSE DE LA SOLUTION D’HYDROXYDE DE SODIUM :
III-2-1/ EXPERIENCE :
Réalisons le circuit ci-dessous. L’électrolyseur contient une solution d’hydroxyde de sodium.
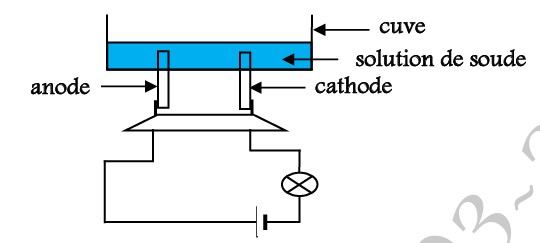
III-2-2/ OBSERVATION :
On constate que l’ampoule brille quand on forme l’interrupteur
III-2-3/ INTERPRETATION :
La solution d’hydroxyde de sodium conduit le courant électrique donc elle contient des ions. Lors de la dissolution, l’eau a totalement dissociée les cristaux d’hydroxyde de sodium selon l’équation-bilan:
![]()
III-2-4/ CONCLUSION :
La solution d’hydroxyde de sodium contient alors des ions hydroxydes (HO-) et des ions sodiums (Na+).
N.B:
► Les ions hydroxydes (HO-) sont responsables du caractère basique d’une solution basique.
► La solution d’hydroxyde de sodium sera notée: (Na+ + HO-)
III-3/ PROPRIETES LIEES A L’ION HYDROXYDE (HO-) :
III-3-1/ ACTION SUR LES IONS METALLIQUES :
Les ions hydroxydes réagissent avec les ions métalliques (Zn2+, Al 3+, Fe2+, Pb2+, Cu2+…) pour donner des précipités d’hydroxyde métallique.
Exemples:
► Réaction entre l’ion hydroxyde et l’ion métallique (Zn2+):
![]()
► Réaction entre l’ion hydroxyde et l’ion métallique (Al 3+):
![]()
III-3-2/ ACTION SUR LES INDICATEURS COLORES :
► Expérience :
Considérons trois tubes à essais contenant chacun une solution d’hydroxyde de sodium. Puis ajoutons dans chaque tube un indicateur coloré (hélianthine tube 1 ; phénolphtaléine tube 2 et B.B.T tube 3).

► Observations :

On constate que la solution dans le tube (1) vire au jaune ; la solution dans le tube (2) vire au rouge violacée et la solution dans le tube (3) vire au bleu.
► Interprétation :
Les couleurs obtenus caractérisent la présence des ions hydroxydes (HO-) dans ces solutions.
III-3-3/ ACTION SUR LES ACIDES :
Les ions hydroxydes (HO-) réagissent mole à mole avec ions hydroniums (H3O+) suivant une réaction totale en donnant de l’eau. Cette réaction dégage aussi de la chaleur: elle est dite exothermique.
L’équation bilan de la réaction s’écrit:
![]()
C’est une réaction rapide, totale est exothermique.
III-3-4/ CARACTERISATION DE L’ION SODIUM (NA+): TEST A LA FLAMME :
Un fil de platine préalablement trempé dans une solution d’hydroxyde de sodium colore en jaune la flamme d’un bec bunsen. Cette coloration jaune est caractéristique de l’élément sodium: la solution d’hydroxyde de sodium contient des ions sodium Na+.
IV/ BASES COURANTES ET BASES TIREES DES PRODUITS LOCAUX:
IV-1/ DEFINITION D’UNE BASE:
Un base est une espèce chimique capable de libérer un ou plusieurs ion (s) HO- en solution aqueuse.
On distingue les monobases et les polybases:
► Lorsqu’une mole de base peut libérer une mole d’ions HO- : la base est qualifiée de monobase.
Exemples:
► Lorsqu’une mole de base peut libérer deux moles d’ions HO-: la base est qualifiée de dibase
Exemples:
► Lorsqu’une mole de base peut libérer trois moles d’ions HO-: la base est qualifiée de tribase.
Exemples:
IV-2/ LES BASES COURANTES :
IV-2-1/ EXPERIENCE :
Considérons trois tubes à essais contenant respectivement une solution d’hydroxyde de potassium, une solution d’hydroxyde de calcium et une solution d’hydroxyde de d’aluminium. Dans chaque tube, introduisons quelques gouttes de Bleu de Bromothymol (B.B.T).
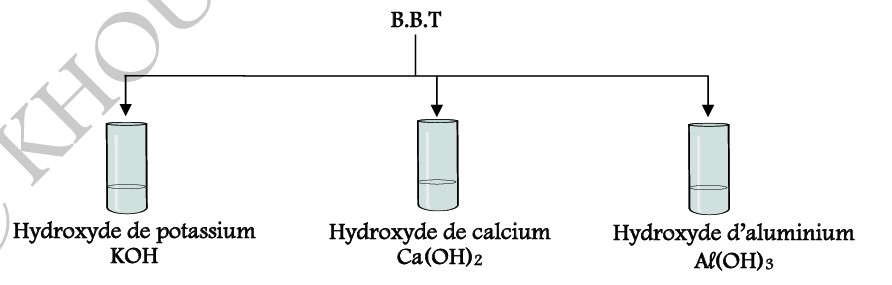
IV-2-2/ OBSERVATIONS :
On constante que toutes les solutions de bases font virer le B.B.T au bleu.

IV-2-3/ INTERPRETATION :
Les solutions d’hydroxyde de potassium, d’hydroxyde de calcium et d’hydroxyde de d’aluminium contiennent tous des ions hydroxydes (HO-): ce sont donc des bases.
IV-3/ LES BASES TIREES DES PRODUITS LOCAUX :
IV-3-1/ EXPERIENCE :
Considérons trois tubes à essais contenant respectivement des solutions de lessive, des cendres et de la craie.
Puis ajoutons dans chaque tube du B.B.T.

IV-3-2/ OBSERVATIONS :
On constante que toutes ces solutions font virer le B.B.T au bleu.

IV-3-3/ INTERPRETATION :
Ces extraits naturels contiennent tous des ions hydroxydes (HO-): ce sont donc des bases.
You must be logged in to take the quiz.

