I/ NOTION DE pH :
I-1/ RELATION [ H3O+ ] = 10 – pH :
Les solutions aqueuses sont caractérisées par leur concentration en ions hydronium H3O+ ou de façon plus commode par leur pH.
Ainsi, le pH et la concentration en ion hydronium d’une solution aqueuse sont liés par la relation :![]()
I-2/ MESURE DU pH D’UNE SOLUTION AQUEUSE :
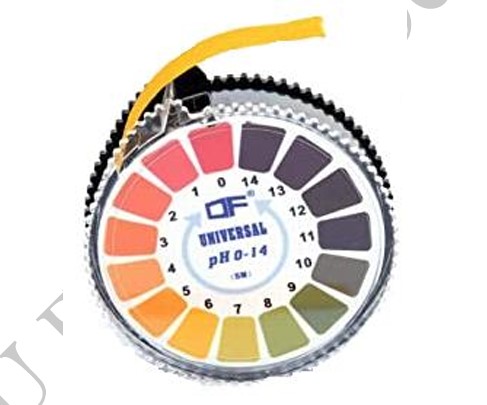
I-2-1/ LE PAPIER pH :
En versant quelques gouttes de la solution aqueuse sur le papier pH, ce dernier prend une couleur qui par comparaison avec la gamme de couleur qui accompagne le rouleau désigne l’ordre de grandeur du pH.
Un papier pH permet une détermination rapide et approchée du pH d’une solution.
I-2-2/ LE pH-METRE :
Le pH-mètre est un appareil électronique relié à une sonde. Lorsque la sonde est plongée dans la solution, l’écran du pH mètre affiche la valeur du pH de la solution.
Le pH-mètre permet une détermination précise du pH d’une solution.

I-3/ LE pH DE L’EAU PURE :
La mesure du pH de l’eau pure à 25 °C donne : pH = 7.
La concentration en ions hydroniums H3O+ de l’eau pure à 25 °C est :
N.B :
Les ions hydroniums H3O+ présents dans l’eau pure sont engendrés par la réaction d’autoprotolyse de l’eau :
REMARQUE :
La réaction d’autoprotolyse montre que dans l’eau pure il y’a autant d’ions hydronium H3O+ que d’ions hydroxyde OH -.![]()
I-4/ PRODUIT IONIQUE DE L’EAU A 25 °C :
Pour une température donnée, le produit entre la concentration des ions hydronium H3O+ et celle des ions hydroxyde OH – est une constante appelée produit ionique de l’eau. Il est noté Ke.![]()
A 25 °C, le produit ionique de l’eau est égal à : Ke = 10 – 14
I-5/ DOMAINE DE pH DES SOLUTIONS A 25 °C :
Toute solution aqueuse à une valeur de pH comprise entre 0 et 14.![]()
I-5-1/ DOMAINE DE pH D’UNE SOLUTION ACIDE :
Toute solution acide à 25 °C à une valeur de pH inférieure à 7.![]()
N.B : une solution acide renferme plus d’ions hydroniums H3O+ que d’ions hydroxydes OH –
I-5-2/ DOMAINE DE pH D’UNE SOLUTION BASIQUE :
Toute solution basique à 25 °C à une valeur de pH supérieure à 7.![]()
N.B : une solution basique renferme plus d’ions hydroxydes OH – que d’ions hydroniums H3O+

II/ INDICATEURS COLORES, ZONE DE VIRAGE :
II-1/ DEFINITION :
On appelle indicateur coloré une substance organique qui peut donner trois couleurs différentes suivant la nature de la solution (acide, basique ou neutre) dans laquelle il est introduit.
II-2/ TEINTES ACIDE, BASIQUE, ET SENSIBLE :
II-2-1/ EXPERIENCE :
Considérons trois tubes à essai (1) ; (2) et (3) contenant respectivement des solutions d’hydroxyde de sodium (Na+ ; HO-) ; d’acide chlorhydrique (H3O+ ; Cl -) et du chlorure de sodium (Na+ ; Cl -). Versons quelques gouttes de bleu de bromothymol (indicateur coloré) dans chaque tube.

II-2-2/ OBSERVATIONS :

On observe :
Dans le tube (1) contenant l’hydroxyde de sodium, le BBT vire à sa coloration bleue.
Dans le tube (2) contenant d’acide chlorhydrique, le BBT vire à sa coloration jaune.
Dans le tube (3) contenant le chlorure de sodium, le BBT vire à sa coloration verte.
II-2-3/ INTERPRETATION :
La coloration bleue du BBT dans le tube (1) caractérise sa teinte en milieu basique.
La coloration jaune du BBT dans le tube (2) caractérise sa teinte en milieu acide.
La coloration verte du BBT dans le tube (3) caractérise sa teinte en milieu neutre (sensible).
II-3/ ZONE DE VIRAGE :
On appelle zone de virage d’un indicateur coloré, la zone de pH dans laquelle aucune des deux teintes (acide et base) de l’indicateur n’est majoritaire.

III/ DOSAGE D’UNE SOLUTION D’ACIDE CHLORHYDRIQUE PAR LA SOUDE :
III-1/ DEFINITION :
Le dosage d’une solution consiste à déterminer sa concentration molaire.
III-2/ DOSAGE D’UNE SOLUTION D’ACIDE CHLORHYDRIQUE PAR LA SOUDE :
III-2-1/ DISPOSITIF EXPERIMENTAL :
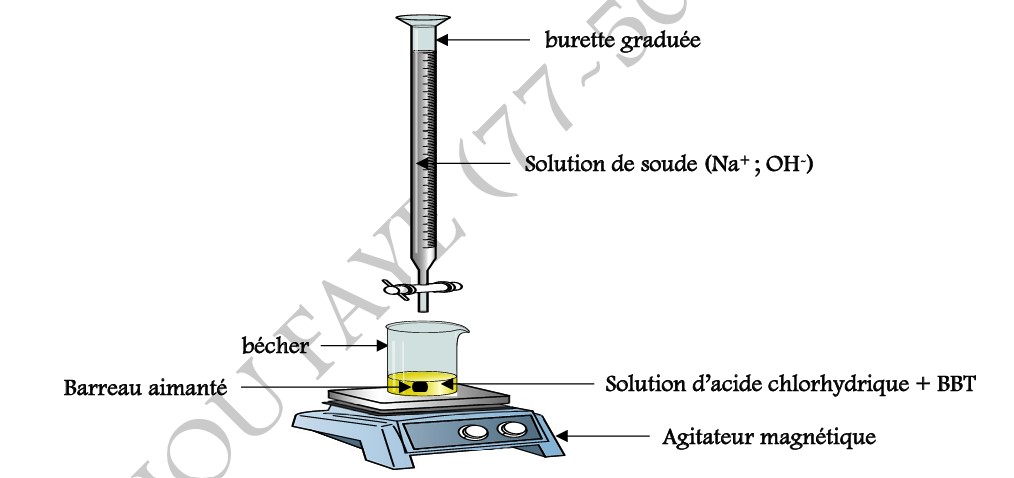
III-2-2/ PRINCIPE DU DOSAGE :
Le principe consiste à verser dans le bécher contenant un volume VA d’acide chlorhydrique goutte à goutte la solution de soude contenue dans la burette jusqu’à ce que la solution dans le bécher passe du jaune au vert. Soit VB le volume de soude versé.
Ce changement brusque de couleur correspond à l’équivalence acido-basique du dosage.
III-2-3/ EQUATION BILAN DE LA REACTION DU DOSAGE :

III-2-4/ NOTION D’EQUIVALENCE ACIDO-BASIQUE :
On appelle équivalence acido-basique le moment du dosage pour lequel le nombre de mole de H3O+ est égale au nombre de mole de HO-.
Autrement dit c’est lorsque l’acide et la base sont dans les proportions stœchiométriques.

A l’équivalence acido-basique : CAVA = CBVB ⇒

You must be logged in to take the quiz.

