I/ ETATS PHYSIQUES ET CHANGEMENT D’ETAT :
I-1/ ETATS PHYSIQUES DE LA MATIERE :
La matière (substance qui constitue les corps) se présente dans la nature sous trois états physiques différents:
l’état solide, l’état liquide et l’état gazeux.
► Les solides : ils ont une forme propre.
Exemples: bois, règle, glace etc. …
► Les liquides : ils coulent et prennent la forme du récipient qui les contient : ils n’ont pas de forme propre.
La surface d’un liquide au repos (immobile) est plane et horizontale.
Exemples: eau, huile, mercure, boisson etc. …
► Les gaz : l’air qui nous entoure est un gaz. Un gaz s’échappe d’un récipient ouvert et occupe tout le
volume qui lui est offert.
I-2/ CHANGEMENT D’ETATS PHYSIQUES :
I-2-1/DEFINITION :
On appelle changement d’état physique, le passage d’un état physique donné à un autre état physique.
I-2-2/ DIAGRAMME DE CHANGEMENT D’ETAT :

REMARQUE :
Un changement d’état physique s’effectue toujours à une température constante sous une pression donnée.
I-3/ TRANSFORMATION DE LA MATIERE :
I-3-1/ PHENOMENE PHYSIQUE :
Un phénomène physique est une transformation au cours de laquelle la nature de la matière n’est pas altérée(détruite, faussée, dénaturée).
Exemples: fusion de la glace, dilatation d’un mercure dans un thermomètre, la rosée …
I-3-2/ PHENOMENE CHIMIQUE :
Un phénomène chimique est une transformation au cours de laquelle la nature de la matière est altérée.
Exemples: feuille de papier brûlé, combustion d’une bougie, la rouille du fer…
II/ MELANGES ET PROCEDES DE SEPARATION :
II-1/ MELANGES :
II-1-1/ DEFINITION :
Un mélange est un ensemble de deux ou plusieurs substances dont chacun garde ces mêmes propriétés
physiques et chimiques.
II-1-2/ TYPES DE MELANGES :
On distingue deux types de mélanges : le mélange homogène et le mélange hétérogène.
►Mélange homogène: un mélange homogène est un mélange dans lequel on ne peut pas distinguer à l’œil nu ses différents constituants.
Un tel mélange présente une seule phase.
Exemples: eau + sel ; l’air ; eau + alcool ; eau + sucre….
►Mélange hétérogène: un mélange est hétérogène lorsqu’à l’œil nu on peut distinguer ses différents
constituants.
Exemples: sable + sucre ; huile + eau ; eau + sable…
II-2/ METHODES DE SEPARATION D’UN MELANGE :
Pour rendre limpides les eaux usées, celles des marigots, des puits,…, on peut utiliser différents procédés de séparation que sont:
II-2-1/ LA DECANTATION :
La décantation est une méthode de séparation liquide-solide basée sur la différence de densités des corps.
Elle consiste à laisser le mélange au repos, les particules solides lourdes se déposent lentement au fond. En versant avec précaution (transvaser), on peut séparer le liquide de ces particules.

REMARQUE :
L’eau décantée est un mélange hétérogène non pur car elle contient des particules légères.
II-2-2/ LA FILTRATION :
La filtration est une méthode de séparation basée sur la différence de la grosseur des particules. Elle consiste à verser le mélange liquide (eau décantée) dans un filtre en papier placé sur un entonnoir. On recueille, après traversée du filtre, un liquide limpide: c’est le filtrat.
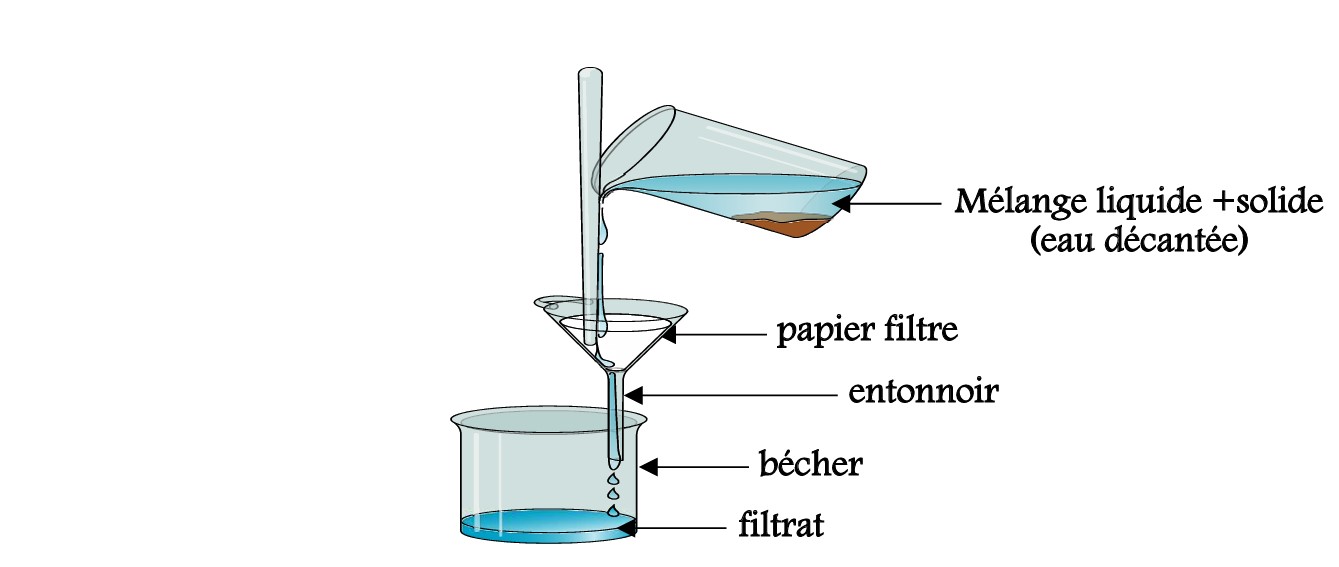
REMARQUE :
Le filtrat est un mélange homogène non pur car elle contient des particules finement divisées.
II-2-3/ LA DISTILLATION :
La distillation est une méthode de séparation basée sur la différence de températures d’ébullition
(température à laquelle bout un corps) des différents constituants. Elle consiste à chauffer le mélange
homogène jusqu’à l’ébullition dans un ballon. La vapeur obtenue est conduite dans un réfrigérant (refroidie par un courant d’eau) où elle se liquéfie. Le liquide recueilli à la sortie du réfrigérant est appelé distillat ou liquide distillé.
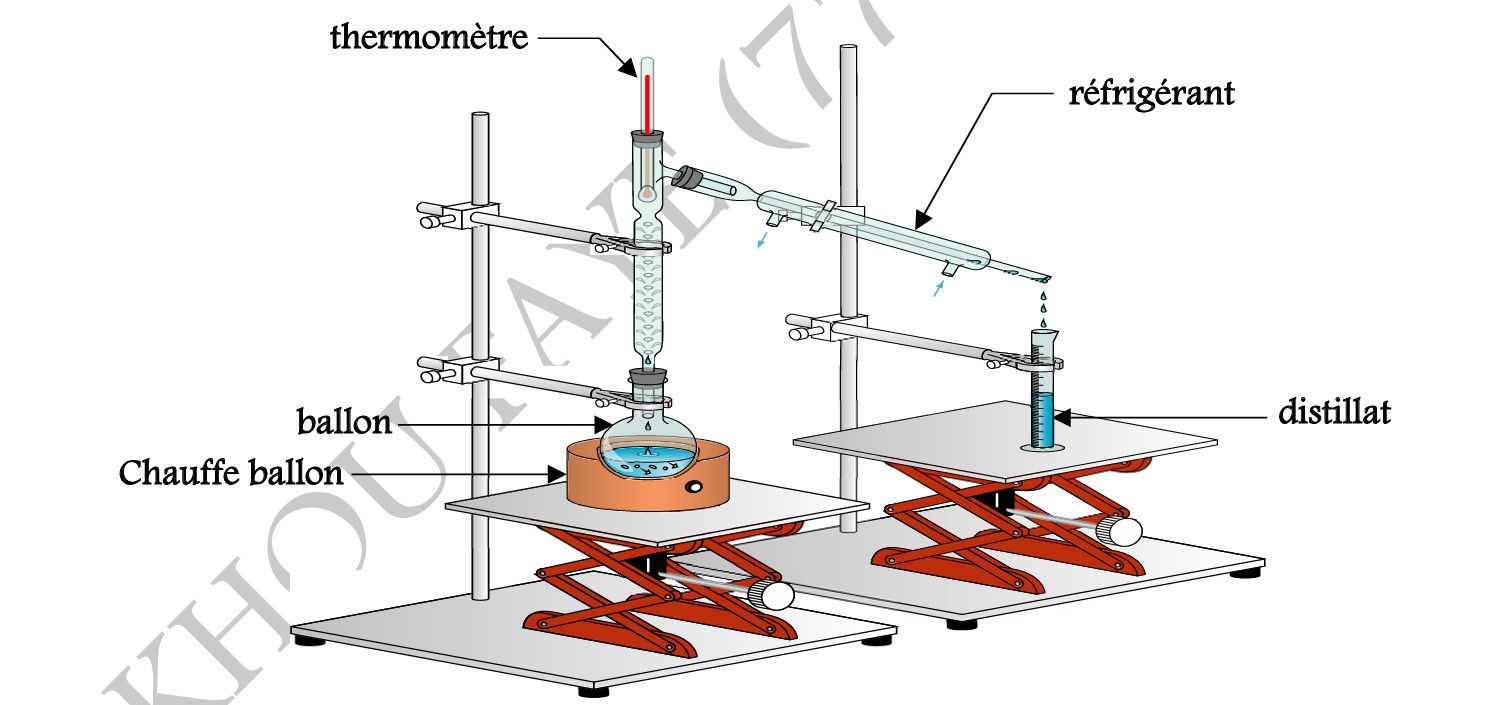
REMARQUE :
Seul le corps dont on atteint sa température d’ébullition est recueilli: ce corps est pur.
La distillation n’est possible que lorsque les corps ont des différences de température d’ébullition supérieures ou égale à 3°C.
III/ CORPS PURS :
III-1/ DEFINITION :
Un corps pur est un corps qu’on ne peut pas fractionner par une quelconque méthode de séparation ; c’est à-dire toutes les parties d’un corps pur sont identiques.
III-2/ CARACTERISTIQUES D’UN CORPS PUR :
Un corps pur est caractérisé par ces critères de pureté qui sont des constantes physiques telles que la
température de fusion ; la température d’ébullition ; la masse volumique… .
► Les températures de changement d’état physique :
Pour un corps pur, le changement d’état physique se fait à une température constante.
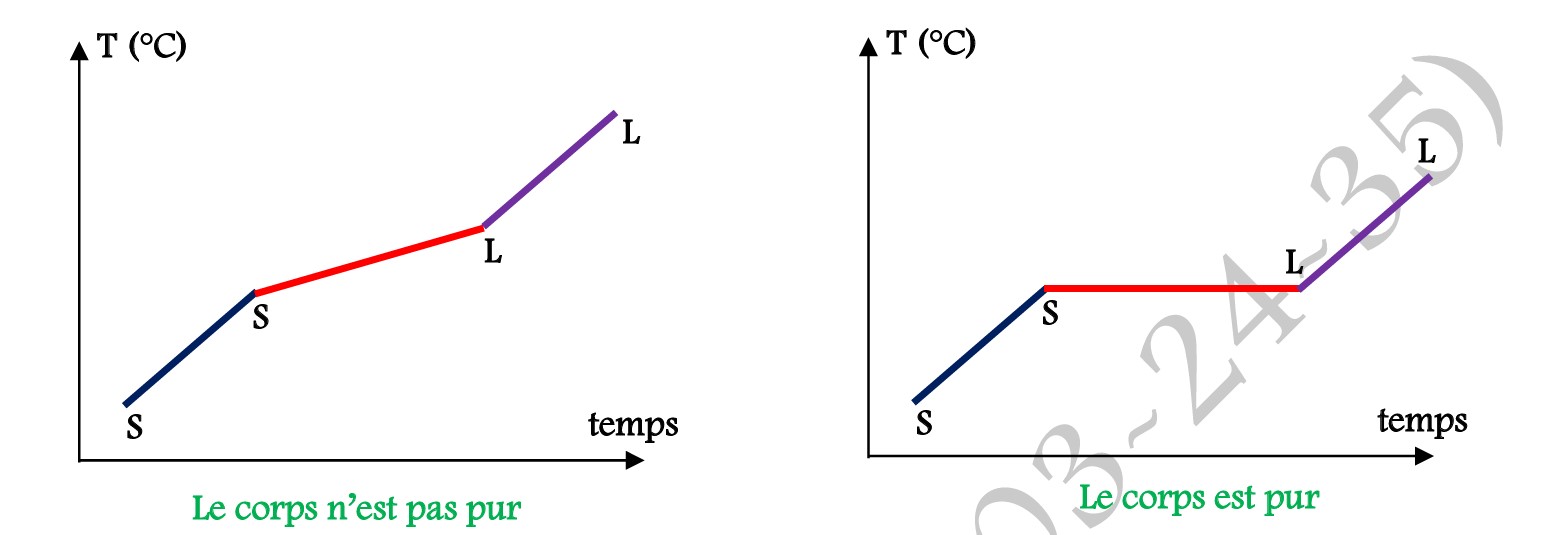
► La masse volumique :
La masse volumique d’un corps est égale à la masse (m) de ce corps sur son volume (V). Elle est notée P (rho) ou µ (mu) et s’exprime en kg.m-3 dans le système international.
Elle est donnée par l’expression:

La masse volumique d’un corps pur est constante.
![]()
IV/ ANALYSE ET SYNTHESE DE L’EAU :
IV-1/ ANALYSE DE L’EAU :
IV-1-1/ DEFINITION :
Analyser un corps revient à chercher ses constituants par une méthode appropriée. L’appareil utilisé pour réaliser l’analyse de l’eau est appelé électrolyseur.
IV-1-2/ DISPOSITIF EXPERIMENTAL :
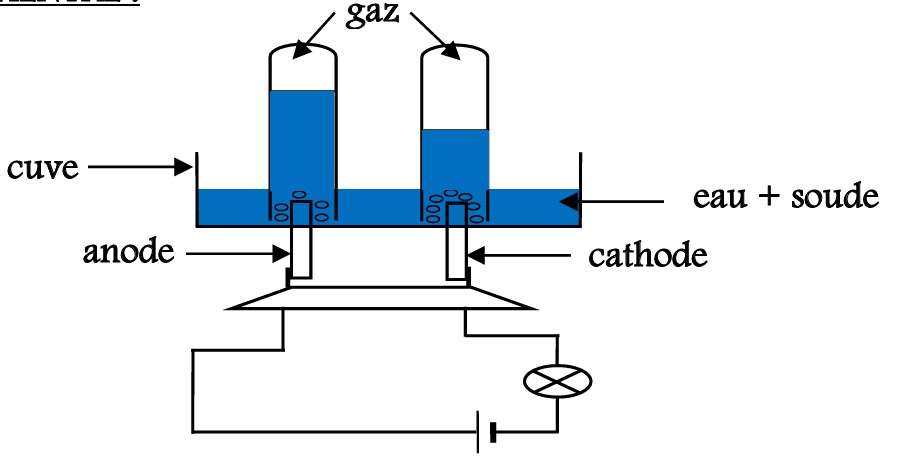
Versons de l’eau additionnée de soude dans la cuve de l’électrolyseur puis fermons l’interrupteur.
IV-1-3/ OBSERVATIONS :
On constate que la lampe s’allume et un dégagement de bulles de gaz au niveau des électrodes: ces bulles
de gaz montent dans les tubes.
IV-1-4/ IDENTIFICATION DES GAZ :
Approchons un brin d’allumette incandescent aux deux tubes.

► A la cathode ; l’électrode reliée au pôle négatif du générateur : il se dégage un gaz qui brûle avec une
faible détonation ou explosion : c’est le dihydrogène (H2).
► A l’anode ; l’électrode reliée au pôle positif du générateur : il se dégage un gaz qui entretient la
combustion: c’est le dioxygène (O2).
N.B:
Des expériences ont montré que le volume de dihydrogène est le double du volume de dioxygène.
IV-1-5/ CONCLUSION :
La décomposition de l’eau pure donne deux gaz: le dihydrogène et le dioxygène qui sont également des
corps purs.
IV-2/ SYNTHESE DE L’EAU :
IV-2-1/ DEFINITION :
Faire la synthèse de l’eau c’est reconstituer l’eau à partir de ses différents constituants. L’appareil utilisé
pour réaliser la synthèse de l’eau est appelé eudiomètre.
IV-2-2/ DISPOSITIF EXPERIMENTAL :
Mélangeons dans un eudiomètre du dihydrogène et du dioxygène tel que V(H2) soit le double de V(O2)
puis faisons passer une étincelle électrique.
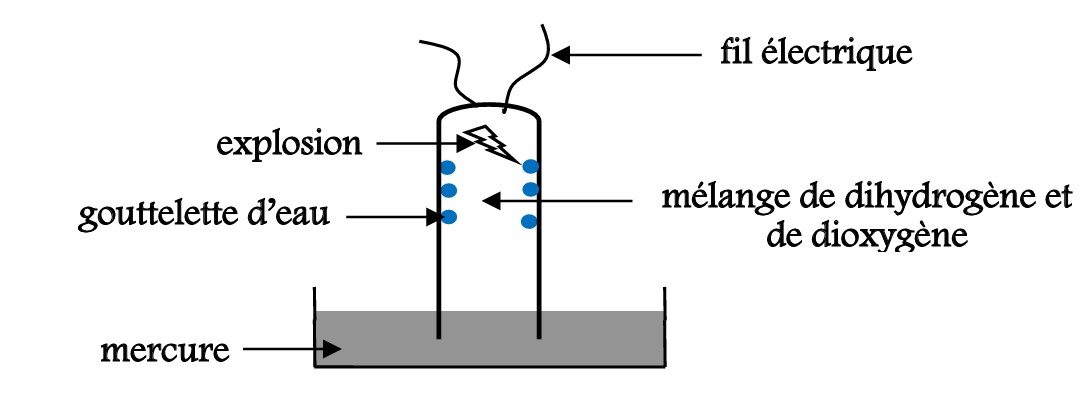
IV-2-3/ OBSERVATIONS :
On constate une petite explosion suivie de la formation de gouttelettes d’eau sur les parois interne du tube.
IV-2-4/ CONCLUSION :
On a reconstituée l’eau à partir du dihydrogène et du dioxygène.
IV-3/ CORPS PURS COMPOSES ET CORPS PURS SIMPLES :
IV-3-1/ CORPS PURS COMPOSES :
C’est un corps pur qu’on peut décomposer en d’autres corps purs.
Exemples: eau ; sucre ; butane…
IV-3-1/ CORPS PURS SIMPLES :
C’est un corps pur qu’on ne peut pas décomposer en d’autres corps purs.
Exemples: le dihydrogène ; le dioxygène ; l’ozone…
V/ AUTRES EXEMPLES DE MELANGES ET PROCEDES DE SEPARATION :
V-1/ MELANGE SOLIDE-SOLIDE :
Exemple 1: mélange pierres + sable
Pour séparer le mélange pierres + sable on utilise comme méthode de séparation le triage manuel.
Exemple 2: mélange fer + sable
Pour séparer le mélange fer + sable on utilise comme méthode de séparation le triage magnétique.
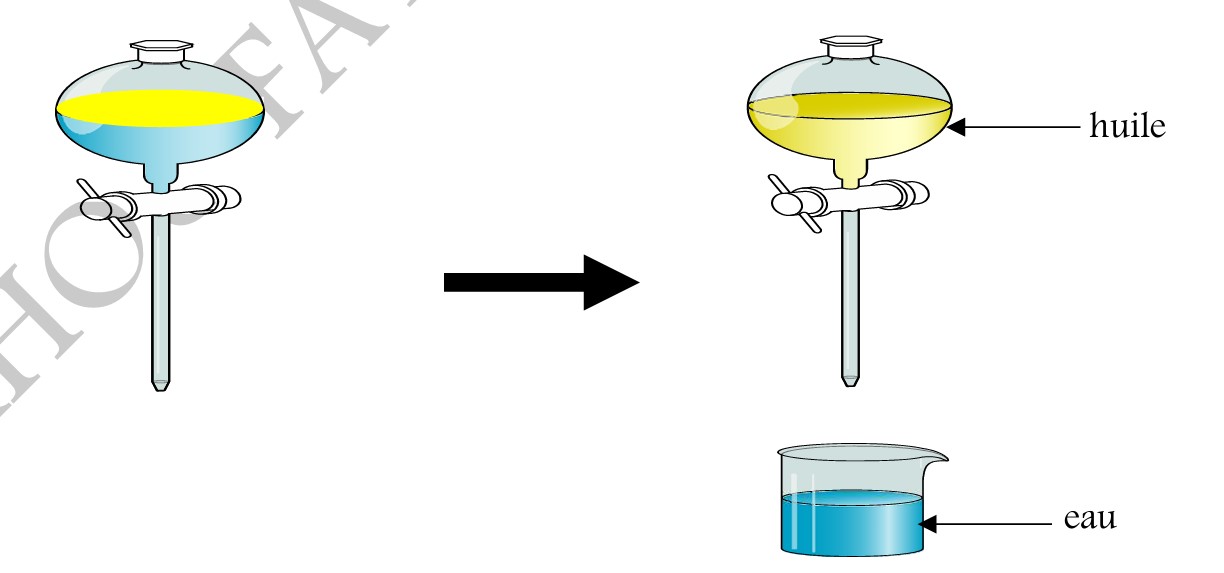
V-2/ MELANGE LIQUIDE-LIQUIDE NON MISCIBLES :
Exemple: mélange eau + huile
Deux liquides non miscibles sont deux liquides qui ne se mélangent pas parfaitement: ils forment un
mélange hétérogène.
Pour séparer un mélange eau + huile, on effectue une décantation avec une ampoule à décanter.
V-3/ MELANGE GAZEUX: L’AIR :
L’air est un mélange gazeux formé de 78% de diazote, 21% de dioxygène et 1% d’autres gaz.
You must be logged in to take the quiz.


